
Back أحادي نوكليوتيد الفلافين Arabic فلاوین مونونوکلئوتید AZB Riboflavin-5'-fosfat BS Mononucleòtid de flavina Catalan Flavinmononukleotid German Flavin mononucleotide English Flavín mononucleótido Spanish فلاوین مونونوکلئوتید FA Flaviinimononukleotidi Finnish Flavine mononucléotide French
| Flavinmononukleoktid | |
|---|---|
 | |
| Obecné | |
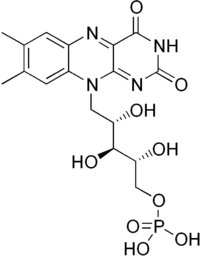
| Systematický název | oxidovaný: 7,8-dimethyl-10-(5-fosfo-D-ribityl)isoalloxazin redukovaný: (dihydroriboflavin-5′-fosfát)-1,5-dihydro-7,8-dimethyl-10-(5-fosfo-D-ribityl) isoalloxazin[1] |
| Triviální název | Flavinmononukleoktid |
| Sumární vzorec | C17H21N4O9P |
| Identifikace | |
| Registrační číslo CAS | 146-17-8 |
| Vlastnosti | |
| Molární hmotnost | 456,344 g/mol |
Některá data mohou pocházet z datové položky. | |
Flavinmononukleoktid (FMN, riboflavin-5'-fosfát) je biomolekula produkovaná z riboflavinu (vitamin B2) enzymem riboflavinkinázou a funguje jako kofaktor nebo prostetická skupina[2] různých oxidoreduktáz (včetně NADH dehydrogenázy). Jako oxidačně-redoxně[3] aktivní sloučenina je řazena mezi flavinové nukleotidy.[1] Od příbuzné sloučeniny flavinadenindinukleotid (FAD) se liší nepřítomností adenosinmonofosfátu (AMP).
Přestože se FMN nazývá flavinmononukleotid, nejedná o nukleotid. Isoalloxazinový skelet není navázán na ribózu, ale na ribitol, a spojení není realizováno glykosidovou vazbou.
FMN je oxidačně-redoxně aktivní sloučenina, která přechází z oxidované chinonové (FMN) přes semichinonovou formu (FMNH•) na hydrochinonovou formu (FMNH•). Existence tří oxidačních stavů je důležitá pro propojení různých oxidačně-redukčních drah. K redukci dochází na dvou dusíkových atomech v heterocyklických kruzích flavinu. FMN je silnější oxidační činidlo než NAD a je zvláště užitečný, protože se může účastnit přenosů jednoho i dvou elektronů.
FMN je součástí flavoproteinů a je kofaktorem například v komplexu I (NADH dehydrogenáza) v dýchacím řetězci. V roce 1937 obdržel Paul Karrer Nobelovu cenu za svou základní práci o skupině látek flavinů.
- ↑ a b Oxford dictionary of biochemistry and molecular biology; revised edition. Příprava vydání R. Cammack et al. New York: Oxford university press, 2006. ISBN 0-19-852917-1.
- ↑ VODRÁŽKA, Zdeněk; RAUSCH, Pavel; KÁŠ, Jan. Enzymologie. [s.l.]: VŠCHT v Praze, 1998.
- ↑ VOET, Donald; VOET, Judith. Biochemie. 1.. vyd. Praha: Victoria Publishing, 1995. ISBN 80-85605-44-9.