
Back ثلاثي كلورو فلورو الميثان Arabic تریکولوروفلوئورومتان AZB Triclorofluorometà Catalan Trichlorfluormethan Czech Trichlorofluoromethane English تریکلروفلوئورومتان FA Trikloorifluorimetaani Finnish Trichlorofluorométhane French Fluor-triklórmetán Hungarian Triclorofluorometano Italian
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
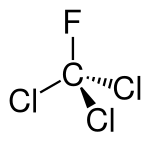
| Name | Trichlorfluormethan | ||||||||||||||||||
| Andere Namen |
| ||||||||||||||||||
| Summenformel | CCl3F | ||||||||||||||||||
| Kurzbeschreibung |
nicht brennbare farblose Flüssigkeit oder Gas mit etherischem Geruch[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 137,37 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
flüssig[1] | ||||||||||||||||||
| Dichte |
1,479 g·cm−3 (flüssig)[1] | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Siedepunkt |
23,6 °C[1] | ||||||||||||||||||
| Dampfdruck | |||||||||||||||||||
| Löslichkeit | |||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| MAK | |||||||||||||||||||
| Treibhauspotential |
5352 (bezogen auf 100 Jahre)[4] | ||||||||||||||||||
| Thermodynamische Eigenschaften | |||||||||||||||||||
| ΔHf0 |
−301,3 kJ/mol[5] | ||||||||||||||||||
| Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||||||||
Trichlorfluormethan ist eine chemische Verbindung der Fluorchlorkohlenwasserstoffe (FCKW), die für ihre Verwendung als Kältemittel R-11 oder als Treibgas bekannt ist. Da es wie alle FCKW die Ozonschicht zerstört, wird es mehr und mehr durch umweltfreundlichere Stoffe ersetzt.
- ↑ a b c d e f g h i j k l Eintrag zu Trichlorfluormethan in der GESTIS-Stoffdatenbank des IFA, abgerufen am 20. Januar 2022. (JavaScript erforderlich)
- ↑ Donald J. Burton, Vinod Jairaj: Trichlorofluoromethane. In: Encyclopedia of Reagents for Organic Synthesis. DOI:10.1002/047084289X.rn00550.
- ↑ Schweizerische Unfallversicherungsanstalt (Suva): Grenzwerte – Aktuelle MAK- und BAT-Werte (Suche nach 75-69-4 bzw. Trichlorfluormethan), abgerufen am 2. November 2015.
- ↑ G. Myhre, D. Shindell, F.-M. Bréon, W. Collins, J. Fuglestvedt, J. Huang, D. Koch, J.-F. Lamarque, D. Lee, B. Mendoza, T. Nalajima, A. Robock, G. Stephens, T. Takemura, H. Zhang et al.: Climate Change 2013: The Physical Science Basis. Working Group I contribution to the IPCC Fifth Assessment Report. Hrsg.: Intergovernmental Panel on Climate Change. 2013, Chapter 8: Anthropogenic and Natural Radiative Forcing, S. 24–39; Table 8.SM.16 (PDF).
- ↑ David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 90. Auflage. (Internet-Version: 2010), CRC Press / Taylor and Francis, Boca Raton FL, Standard Thermodynamic Properties of Chemical Substances, S. 5-19.
