Our website is made possible by displaying online advertisements to our visitors.
Please consider supporting us by disabling your ad blocker.
Chlorid sulfurylu
| Chlorid sulfurylu | |
|---|---|
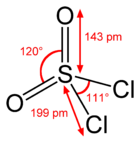 Struktura molekuly chloridu sulfurylu | |
 Kapalná forma | |
| Obecné | |
| Systematický název | chlorid sulfurylu |
| Ostatní názvy | sulfurylchlorid dichlorid-dioxid sírový |
| Anglický název | Sulfuryl chloride |
| Německý název | Sulfurylchlorid |
| Sumární vzorec | SO2Cl2 |
| Vzhled | bezbarvá kapalina (postupem času žloutnoucí) |
| Identifikace | |
| Registrační číslo CAS | 7791-25-5 |
| EC-no (EINECS/ELINCS/NLP) | 232-245-6 |
| Indexové číslo | 016-016-00-6 |
| Vlastnosti | |
| Molární hmotnost | 134,971 g/mol |
| Teplota tání | −54,1 °C |
| Teplota varu | 69,1 °C |
| Teplota rozkladu | 160 °C |
| Hustota | 1,709 1 g/cm3 (0 °C) 1,66 g/cm3 (20 °C) 1,657 0 g/cm3 (25 °C) |
| Index lomu | nD= 1,443 7 |
| Rozpustnost ve vodě | reaguje |
| Rozpustnost v polárních rozpouštědlech | aceton |
| Rozpustnost v nepolárních rozpouštědlech | kapalné uhlovodíky chlorované uhlovodíky sirouhlík |
| Relativní permitivita εr | 9,15 (22 °C) |
| Tlak páry | 5,45 kPa (0 °C) 12,69 kPa (18 °C) 33,61 kPa (39 °C) 51,41 kPa (50 °C) |
| Měrná magnetická susceptibilita | −5,08×10−6 cm3g−1 |
| Struktura | |
| Tvar molekuly | tetraedr |
| Dipólový moment | 6,0×10−30 Cm |
| Termodynamické vlastnosti | |
| Standardní slučovací entalpie ΔHf° | −389,8 kJ/mol |
| Entalpie varu ΔHv | 208 J/g |
| Standardní molární entropie S° | 216,3 JK−1mol−1 |
| Standardní slučovací Gibbsova energie ΔGf° | −305,0 kJ/mol |
| Izobarické měrné teplo cp | 0,973 5 JK−1g−1 |
| Bezpečnost | |
| [1] Nebezpečí[1] | |
| H-věty | H314 H335 EUH014 |
| R-věty | R14 R34 R37 |
| S-věty | (S1/2) S26 S45 |
Některá data mohou pocházet z datové položky. | |
Chlorid sulfurylu (též sulfurylchlorid) (SO2Cl2) je sloučenina síry, kyslíku a chloru. Při pokojové teplotě je to bezbarvá kapalina štiplavého zápachu. Chlorid sulfurylu se nevyskytuje v přírodě, což lze dovodit i z toho, že podléhá rychlé hydrolýze.
Chlorid sulfurylu bývá často zaměňován s chloridem thionylu, SOCl2. Vlastnosti obou oxychloridů síry jsou však podstatně odlišné: chlorid sulfurylu je zdrojem chloru, kdežto chlorid thionylu je zdrojem chloridových iontů.
- ↑ a b Sulfuryl chloride. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-23]. Dostupné online. (anglicky)
Previous Page Next Page




