Our website is made possible by displaying online advertisements to our visitors.
Please consider supporting us by disabling your ad blocker.
Nitrure de carbone graphitique

Le nitrure de carbone graphitique, ou g-C3N4, est un polymorphe de nitrure de carbone, de formule chimique approchée C3N4 omettant une certaine quantité d'hydrogène. Il s'agit d'un ensemble de polymères dont la géométrie moléculaire est bidimensionnelle comprenant des sous-structures de type heptazine et poly(triazine imide) dont le degré de condensation varie en fonction des conditions de formation. Ces matériaux ont des propriétés semiconductrices et catalytiques particulières qui les rendent intéressants par exemple pour l'activation du benzène, les réactions de trimérisation, ou encore l'activation du dioxyde de carbone dans les réactions de photosynthèse artificielle[1].
-
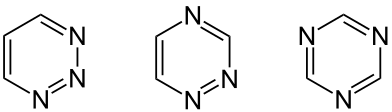
Structure des différentes triazines.
La caractérisation du nitrure de carbone graphitique cristallisé peut être réalisée en identifiant les cycles de triazine du matériau par spectrométrie photoélectronique X (XPS), spectre de photoluminescence et spectroscopie infrarouge à transformée de Fourier (FTIR) (pics à 800 cm−1, 1 310 cm−1 et 1 610 cm−1)[2].
On peut obtenir du nitrure de carbone graphitique par polymérisation de cyanamide N≡C–NH2, de dicyandiamide (2-cyanoguanidine) N≡C–N=C(NH2)2 ou de mélamine C3H6N6. La première structure C3N4 polymérique formée est un polymère très ordonné, avec des groupes amine libres. Si l'on poursuit la réaction, il se forme un composé plus condensé à base d'heptazine C6N7[1]. On peut également préparer le g-C3N4 par cataphorèse d'une solution saturée de mélamine et de chlorure cyanurique (ratio 1:1,5) sur un substrat Si(100) à température ambiante[3]. On a obtenu des nanocristallites de nitrure de carbone graphitique bien cristallisés en faisant réagir du chlorure cyanurique et de l'amidure de sodium NaNH2 de 180 à 220 °C pendant 8 à 12 heures[2]. Une autre méthode consiste à chauffer de 400 à 600 °C un mélange de mélamine C3H6N6 et d'acide urique C5H4O3N4 en présence d'alumine Al2O3 : l'alumine agit en favorisant la formation de nitrure de carbone graphitique sur les surfaces exposées selon une réaction apparentée au dépôt chimique en phase vapeur (CVD) in situ[4].
- (en) Arne Thomas, Anna Fischer, Frederic Goettmann, Markus Antonietti, Jens-Oliver Müller, Robert Schlögl et Johan M. Carlsson, « Graphitic carbon nitride materials: variation of structure and morphology and their use as metal-free catalysts », Journal of Materials Chemistry, vol. 18, no 41, , p. 4893-4908 (DOI 10.1039/B800274F, lire en ligne)
- (en) Qixun Guo, Yi Xie, Xinjun Wang, Shichang Lv, Tao Hou et Xianming Liu, « Characterization of well-crystallized graphitic carbon nitride nanocrystallites via a benzene-thermal route at low temperatures », Chemical Physics Letters, vol. 380, nos 1-2, , p. 84-87 (DOI 10.1016/j.cplett.2003.09.009, Bibcode 2003CPL...380...84G, lire en ligne)
- ↑ (en) Li Chao, Cao Chuanbao et Zhu Hesun, « Preparation of graphitic carbon nitride by electrodeposition », Chinese Science Bulletin, vol. 48, no 16, , p. 1737-1740 (DOI 10.1360/03wb0011, Bibcode 2003ChSBu..48.1737L, lire en ligne)
- ↑ (en) Roberto C. Dante, Pablo Martín-Ramos, Adriana Correa-Guimaraes et Jesús Martín-Gil, « Synthesis of graphitic carbon nitride by reaction of melamine and uric acid », Materials Chemistry and Physics, vol. 130, no 3, , p. 1094-1102 (DOI 10.1016/j.matchemphys.2011.08.041, lire en ligne)
Previous Page Next Page