Our website is made possible by displaying online advertisements to our visitors.
Please consider supporting us by disabling your ad blocker.
Acido borico
| Acido borico | |
|---|---|
 | |
 | |
| Nome IUPAC | |
| acido borico | |
| Nomi alternativi | |
| acido ortoborico acido triossoborico(III) | |
| Caratteristiche generali | |
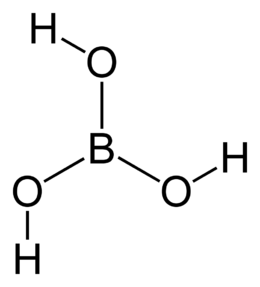
| Formula bruta o molecolare | H3BO3 oppure B(OH)3 |
| Massa molecolare (u) | 61,84 g/mol |
| Aspetto | solido bianco |
| Numero CAS | |
| Numero EINECS | 233-139-2 |
| PubChem | 7628 |
| DrugBank | DBDB11326 |
| SMILES | B(O)(O)O |
| Proprietà chimico-fisiche | |
| Densità (g/cm3, in c.s.) | 1,44 (20 °C) |
| Solubilità in acqua | 46,5 g/l (20 °C) |
| Temperatura di fusione | 171 °C (444 K) (decomposizione) |
| Temperatura di ebollizione | 300 °C (573 K) |
| Indicazioni di sicurezza | |
| Simboli di rischio chimico | |

| |
| pericolo | |
| Frasi H | 360 |
| Consigli P | 201 - 308+313 [1] |
L'acido borico, o acido ortoborico (più raramente acido boracico[2]), ugualmente acido borico nella nomenclatura IUPAC,[3] è un ossiacido del boro trivalente, di formula H3BO3 o B(OH)3 ed è un acido molto debole. Esiste in natura in forma di cristalli incolori o polvere bianca; è solubile in acqua, specialmente a caldo.
È usato spesso come antisettico, insetticida, disinfettante, ritardante di fiamma e in laboratorio per la preparazione di alcune soluzioni, come il TBE (tris-borato-EDTA).
L'acido borico è utilizzato nell'industria del vetro, nella lavorazione degli smalti, delle vernici, della pelle, della carta, degli adesivi e degli esplosivi. È inoltre iniettato nel moderatore delle centrali nucleari BWR o PWR in virtù della natura di assorbitore neutronico di un isotopo del boro per effettuare gli arresti rapidi (SCRAM).
- ^ scheda dell'acido borico su IFA-GESTIS (archiviato dall'url originale il 16 ottobre 2019).
- ^ boracifero, su treccani.it - Vocabolario on line, Istituto dell'Enciclopedia Italiana. URL consultato il 29 maggio 2017.
- ^ (EN) PubChem, Boric Acid, su pubchem.ncbi.nlm.nih.gov. URL consultato il 22 aprile 2024.
Previous Page Next Page


