Our website is made possible by displaying online advertisements to our visitors.
Please consider supporting us by disabling your ad blocker.
Solfuro di zinco
| Solfuro di zinco | |
|---|---|
 | |
 | |
| Nome IUPAC | |
| solfuro di zinco | |
| Caratteristiche generali | |
| Formula bruta o molecolare | ZnS |
| Massa molecolare (u) | 97,43 g/mol |
| Aspetto | solido bianco inodore |
| Numero CAS | |
| Numero EINECS | 215-251-3 |
| PubChem | 14821 |
| SMILES | S=[Zn] |
| Proprietà chimico-fisiche | |
| Densità (g/cm3, in c.s.) | 4,01 (20 °C) |
| Solubilità in acqua | (20 °C) quasi insolubile |
| Temperatura di fusione | 1185 °C (sublima) |
| Proprietà termochimiche | |
| ΔfH0 (kJ·mol−1) | –204,6 |
| Proprietà tossicologiche | |
| DL50 (mg/kg) | >2000 (oral rat)[1] |
| Indicazioni di sicurezza | |
| Frasi H | --[2][1] |
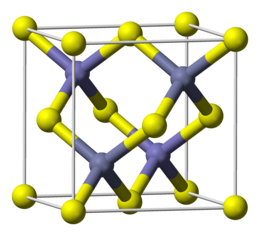
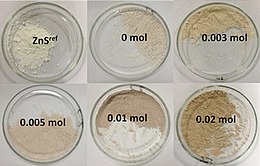
Il solfuro di zinco è il composto inorganico con formula ZnS. È presente in natura principalmente nel minerale sfalerite, oppure nella forma più rara di wurtzite. La sfalerite costituisce la principale fonte industriale di zinco metallico. I minerali sono in genere neri per la presenza di varie impurezze, ma ZnS puro è un solido bianco inodore. ZnS è usato principalmente come pigmento, ma trova applicazione anche come materiale luminescente per fosfori, come semiconduttore e per materiali ottici.
Previous Page Next Page


