
Back Stikstoftetroksied AF رباعي أكسيد ثنائي النتروجين Arabic دینیتروژن تترااوکسید AZB Диазотен тетраоксид Bulgarian Tetraòxid de dinitrogen Catalan Dinitrogentetraoxid Danish Distickstofftetroxid German Dinitrogen tetroxide English Tetróxido de dinitrógeno Spanish دینیتروژن تتراکسید FA
| Peroxyde d'azote | |
 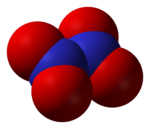 Structure du peroxyde d'azote. |
|
| Identification | |
|---|---|
| Nom UICPA | Tétraoxyde d'azote |
| No CAS | |
| No ECHA | 100.031.012 |
| No CE | 234-126-4 |
| No RTECS | QW9800000 |
| PubChem | 25352 |
| ChEBI | 29803 |
| SMILES | |
| InChI | |
| Apparence | liquide incolore |
| Propriétés chimiques | |
| Formule | N2O4 [Isomères] |
| Masse molaire[1] | 92,011 ± 0,001 6 g/mol N 30,45 %, O 69,55 %, |
| Propriétés physiques | |
| T° fusion | −9,3 °C[2] |
| T° ébullition | 21,15 °C[2] |
| Solubilité | réagit avec l'eau |
| Masse volumique | 1,45 g cm−3 à 20 °C[2] |
| Point critique | 431 K ; 10,1 MPa ; 167 cm3 mol−1[2] |
| Thermochimie | |
| ΔvapH° | 38,12 kJ mol−1 (1 atm, 21,15 °C)[3] |
| Précautions | |
| SGH[4],[5] | |
| H270, H280, H314, H330, P220, P260, P280, P284, P310 et P305+P351+P338 |
|
| SIMDUT[6] | |
Produit non classé |
|
| Transport | |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
Le peroxyde d'azote, ou tétraoxyde de diazote, est un composé chimique de formule N2O4. C'est un liquide incolore à jaune brun selon la concentration de dioxyde d'azote NO2 qu'il contient : N2O4 est en équilibre avec NO2, dont il constitue en fait un dimère. C'est un oxydant très puissant, corrosif et toxique. Appelé également NTO (de l'anglais Nitrogen TetrOxide) en astronautique, le peroxyde d'azote y est très employé comme propergol liquide stockable, notamment avec l'hydrazine et ses dérivés avec lesquels il forme un couple hypergolique.
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- « Nitrogen Tetroxide » dans la base de données Hazardous Substances Data Bank (consulté le 11 juin 2010).
- (en) David R. Lide, CRC Handbook of Chemistry and Physics, Boca Raton, CRC Press/Taylor & Francis, , 90e éd., 2804 p. (ISBN 9781420090840, présentation en ligne).
- Numéro index dans le tableau 3.1 de l'annexe VI du règlement CE no 1272/2008 (16 décembre 2008).
- Sigma-Aldrich.
- « Tétroxyde d'azote » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009.
- « Dinitrogen tetraoxide », sur ESIS, consulté le 11 juin 2010






