
Back كلاثرين Arabic ক্ল্যাথ্রিন Bengali/Bangla Klatrin BS Clatrina Catalan Klathrin Czech Clathrin English Clatrina Spanish کلاترین FA Clathrine French Clatrina GL
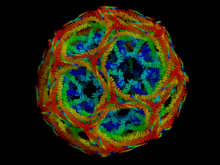
Clathrin ist ein Protein, das an der Einstülpung von Zellmembranen und der Bildung von Vesikeln beteiligt ist (vor allem bei der Clathrin-vermittelten Endozytose). Nach dem Abschnüren wird das Clathrin der Stachelsaumbläschen (clathrin-coated vesicles) ATP-abhängig entfernt („uncoating“ durch die uncoating-ATPase).
Clathrin ist ein außergewöhnlich strukturiertes Protein. Es ist ein Hexamer aus drei schweren und drei leichten Untereinheiten, von denen es je zwei Isoformen gibt. Die Untereinheiten sind in Form eines Dreibeins angeordnet, in Form von Triskelions. Somit ist es möglich, ein zweidimensionales Netzwerk zu bilden, das sich aus Hexagonen und Pentagonen zusammensetzt. Es wird keine flache Ebene erzeugt, sondern ein Konstrukt mit einer konvexen und einer konkaven Seite. Die konkave Seite liegt immer der Membran zugewandt.
Die Clathrin-Vesikel haben Durchmesser von 50 bis 100 nm und werden von einem Gerüst aus meistens 12 Penta- und 8 Hexagonen aus insgesamt 36 Dreifachskeletten von Clathrin überzogen. Dieses fibröse Protein besteht aus einer schweren Kette (180.000 Dalton [Da]) und einer leichten Kette (35.000 bis 40.000 Da). Außerdem kommt das 900 Aminosäuren-lange Dynamin, das GTP binden und hydrolysieren kann, auch im Vesikelmantel vor. Zwischen dem Clathrin und der äußeren Vesikelmembran finden sich sogenannte Adaptorproteinkomplexe (engl. adaptor protein complexes), abgekürzt AP-Komplexe. Diese Komplexe, AP-1 bis AP-4 (≈340.000 Da), bestehen aus je vier unterschiedlichen Polypeptiden, sind also Heterotetramere. Sie binden an die schweren Ketten des Clathrins, Membranlipide sowie Membranproteine und vermitteln dadurch die Clathrin-Bindung an Membranen. AP-2 vermittelt die Bildung von clathrin-coated vesicles (CCV) an der Plasmamembran. AP-1 vermittelt CCV-Bildung am trans-Golgi-Netzwerk, dem letzten Kompartiment des Proteinsyntheseapparates im sekretorischen Transportweg.